Las reacciones químicas y sus ecuaciones
CN.Q.5.1.13. Interpretar las reacciones químicas como la reorganización y recombinación de los átomos con transferencia de energía, mediante la observación y cuantificación de átomos que participan en los reactivos y en los productos.
CN.Q.5.2.8. Deducir y comunicar que las ecuaciones químicas son las representaciones escritas de las reacciones que expresan todos los fenómenos y transformaciones que se producen.

Las ecuaciones químicas permiten describir con claridad lo que ocurre en una reacción química. Mediante símbolos, números y flechas, muestran qué sustancias reaccionan, qué productos se forman, en qué proporciones participan y bajo qué condiciones se produce el cambio. Este lenguaje simbólico hace posible representar procesos que no se observan directamente, pero que pueden analizarse con precisión científica.
En esta clase se examinará cómo una ecuación química resume la reorganización de los átomos y la transferencia de energía, y cómo cada elemento de su simbología —coeficientes, subíndices, estados físicos y flechas— aporta información esencial para interpretar correctamente una reacción.
Ecuaciones químicas
\[ \text{Gasolina} + \text{oxígeno} \;\rightarrow\; \text{dióxido de carbono} + \text{agua} - \text{energía} \]
\[ 2\,\text{C}_{8}\text{H}_{18}(l) + 25\,\text{O}_{2}(g) \;\rightarrow\; 16\,\text{CO}_{2}(g) + 18\,\text{H}_{2}\text{O}(v) \;-\;\Delta H \]
\[ \text{Reactivos} \rightarrow \text{Productos} - \text{energía} \]
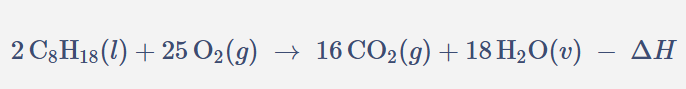
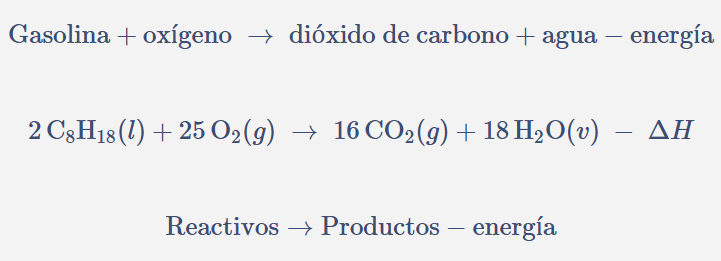
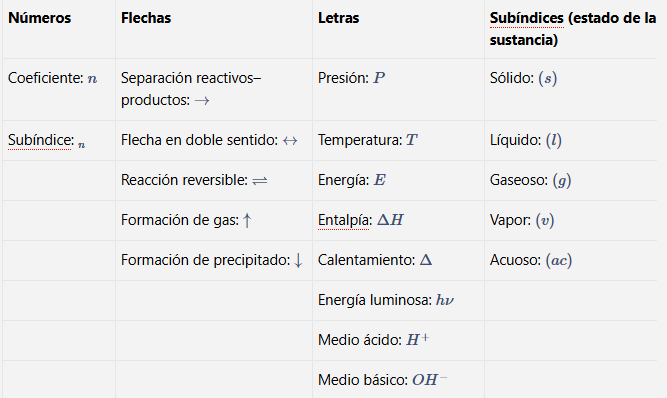
Simbología utilizada en las ecuaciones químicas
Números
Coeficiente
\(n\)
Subíndice
\(_{n}\)
Flechas
Separación de reactivos y productos
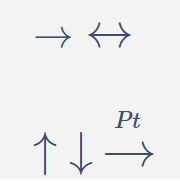
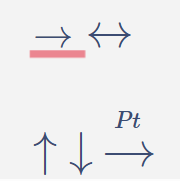
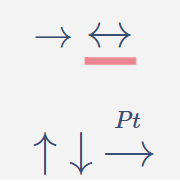
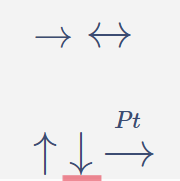
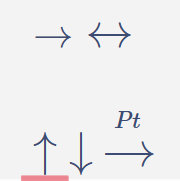
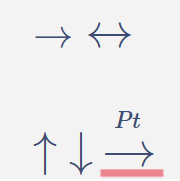
\(\rightarrow\)
Flecha en doble sentido
\(\leftrightarrow\)
Reacción reversible
\(\rightleftharpoons\)
Formación de gas
\(\uparrow\)
Formación de precipitado
\(\downarrow\)
Letras
Presión
\(P\)
Temperatura
\(T\)
Energía
\(E\)
Entalpía
\(\Delta H\)
Calentamiento
\(\Delta\)
Energía luminosa
\(h\nu\)
Catalizador
\(cat.\)
Medio ácido
\(H^{+}\)
Medio básico
\(OH^{-}\)
Subíndices (estado de la sustancia)
Sólido
\((s)\)
Líquido
\((l)\)
Gaseoso
\((g)\)
Vapor
\((v)\)
Acuoso
\((ac)\)
| Números | Flechas | Letras | Subíndices (estado de la sustancia) |
|---|---|---|---|
| Coeficiente: \(n\) | Separación reactivos–productos: \(\rightarrow\) | Presión: \(P\) | Sólido: \((s)\) |
| Subíndice: \({}_{n}\) | Flecha en doble sentido: \(\leftrightarrow\) | Temperatura: \(T\) | Líquido: \((l)\) |
| Reacción reversible: \(\rightleftharpoons\) | Energía: \(E\) | Gaseoso: \((g)\) | |
| Formación de gas: \(\uparrow\) | Entalpía: \(\Delta H\) | Vapor: \((v)\) | |
| Formación de precipitado: \(\downarrow\) | Calentamiento: \(\Delta\) | Acuoso: \((ac)\) | |
| Energía luminosa: \(h\nu\) | |||
| Medio ácido: \(H^{+}\) | |||
| Medio básico: \(OH^{-}\) |
\[ 2\,\text{C}_{8}\text{H}_{18}(l) \]
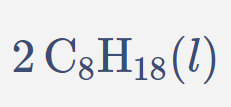
\[ 25 \text{O}_{2} (g) \]
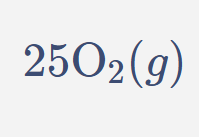
\(\rightarrow\) \(\leftrightarrow\)
\(\uparrow\) \(\downarrow\) \(\xrightarrow{\mathrm{ }_{Pt}}\)
Con esta corta revisión, podemos entender que las ecuaciones químicas son herramientas fundamentales para comunicar los fenómenos químicos. Interpretar adecuadamente su simbología permite reconocer la conservación de la masa, identificar reactivos y productos, y entender el papel de la energía y de las condiciones de reacción.
El dominio de este lenguaje químico facilita el análisis de procesos naturales e industriales y sienta las bases para el estudio de reacciones más complejas. Cada ecuación correctamente interpretada fortalece la comprensión de cómo la materia se transforma de manera ordenada y predecible.