Modelo de Rutherford del átomo nuclear
CN.Q.5.1.3. Observar y comparar la teoría de Bohr con las teorías atómicas de Demócrito, Dalton, Thompson y Rutherford.

Imagina por un momento que pudieras mirar tu mano con un instrumento tan potente que revelara cada átomo que la compone. A simple vista ves algo sólido, compacto, familiar… pero a esa escala extrema aparecería un paisaje casi vacío, un espacio inmenso donde diminutos núcleos y electrones se mueven como puntos de luz. La paradoja es fascinante: percibimos la materia como algo concreto, aunque la mayor parte de un átomo es espacio vacío.
Sucede algo similar cuando observamos radiografías. Una radiografía convierte tu cuerpo en sombras y contrastes, revelando estructuras que normalmente no vemos. Los huesos parecen sólidos y definidos, pero en realidad también están hechos de átomos con grandes espacios vacíos entre ellos. Esto crea un desequilibrio mental interesante, casi como si el mundo nos hiciera un truco: lo sólido no es tan sólido, lo lleno no está tan lleno.
Este tipo de contradicciones abre la puerta al estudio de los modelos atómicos. Desde las ideas filosóficas de Demócrito hasta las propuestas cuantizadas de Bohr, cada teoría intenta explicar cómo es posible que algo “vacío” tenga masa, forma, color y comportamiento. La ciencia avanza afinando estas ideas, comparando evidencias y ajustando lo que creemos saber.
Hoy nos adentraremos, paso a paso, en ese territorio microscópico donde los modelos atómicos dejaron de ser intuiciones y se convirtieron en herramientas para explicar espectros luminosos, reacciones químicas y las leyes que gobiernan la transformación de la materia. Cada modelo será una especie de mapa; juntos forman una cartografía del mundo invisible.
Para poder analizar una estructura tan pequeña como el átomo, se requería de objetos más pequeños que un átomo. A finales del siglo XIX, la ciencia se había embarcado en el estudio de las diversas radiaciones: alfa, beta, gama y radiación X. El común denominador de estas radiaciones era que todas ellas podían atravesar algunos tipos de materia.
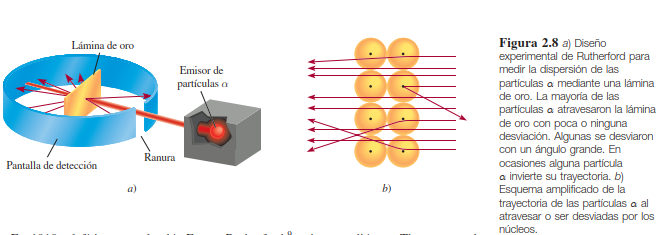 {fig-scap=“Diseño experimental” de Rutherford=“” fig-align=“center”}
{fig-scap=“Diseño experimental” de Rutherford=“” fig-align=“center”}
Descubrimiento del protón
Luego de evidenciar que los electrones, con su carga negativa, eran parte constitutiva de la materia, era lógico pensar en la existencia de una partícula con carga eléctrica positiva, a la que Rutherford llamó protón.
Rutherford evidenció la existencia de los protones, al observar que la radiación estaba constituída de núcleos de helio, es decir, por dos partículas con masa mucho mayor que el electrón y de carga positiva.
| La exploración del átomo es un recordatorio poderoso de que la realidad no siempre coincide con nuestras intuiciones. Lo que parecía indivisible terminó siendo un sistema complejo de partículas; lo que imaginábamos estático resultó dinámico; lo que considerábamos sólido se reveló como un espacio casi vacío organizado por fuerzas y energía. Cada modelo atómico que analizaste hoy representa un momento clave en la aventura intelectual de la humanidad por entender de qué está hecho el universo. |
| Quedan muchos misterios por resolver. El átomo todavía tiene secretos: desde el comportamiento cuántico de los electrones hasta la estructura del núcleo y las interacciones que sostienen la materia. Seguir estudiando estos temas no solo te permite comprender los espectros luminosos o las reacciones químicas, sino también acercarte a una forma más profunda de ver el mundo: una mirada donde lo cotidiano se vuelve extraordinario. |
| La ciencia avanza porque siempre hay alguien dispuesto a hacerse nuevas preguntas. Cada vez que cuestionas lo que “parece evidente”, abres una puerta hacia descubrimientos invisibles a simple vista. Ese impulso es lo que mantiene viva la curiosidad científica. |