Enlace covalente
CN.Q.5.1.9. Observar y clasificar el tipo de enlaces químicos y su fuerza partiendo del análisis de la relación existente entre la capacidad de transferir y compartir electrones y la configuración electrónica, con base en los valores de la electronegatividad.
CN.Q.5.1.10. Deducir y explicar las propiedades físicas de compuestos iónicos y covalentes desde el análisis de su estructura y el tipo de enlace que une a los átomos, así como de la comparación de las propiedades de sustancias comúnmente conocidas.

En química, palabras aparentemente sencillas como ceder y compartir esconden mecanismos profundamente distintos. Cuando un átomo “cede” electrones altera su propia identidad electrónica; cuando “comparte”, establece un equilibrio dinámico con otro átomo en el que ambos participan del mismo par electrón-ico. La diferencia no es solo lingüística: determina la estructura de la materia.
Este será el punto de partida para explorar de manera crítica y rigurosa cómo la electronegatividad y la configuración electrónica gobiernan el tipo y la fuerza de los enlaces, y por qué la materia exhibe comportamientos tan variados.
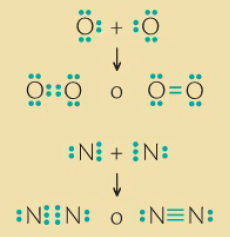
Gilbert Lewis propuso que un átomo podría adquirir una configuración electrónica de gas noble compartiendo electrones con otros átomos.
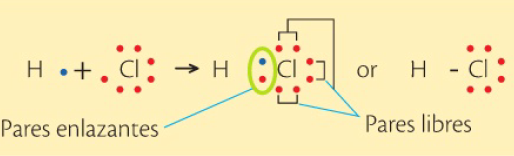
Dependiendo de las parejas de electrones compartidos que se formen, se pueden diferenciar tres tipos de enlace covalente.
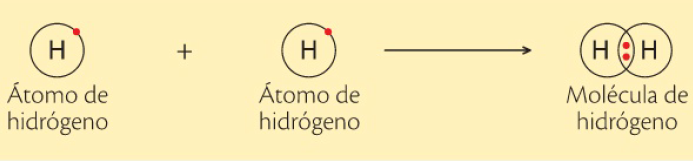


A cada par de electrones compartidos se los puede sustituir con un guion que representa el enlace y los 2 electrones.