El enlace químico
CN.Q.5.1.8. Deducir y explicar la unión de átomos por su tendencia a donar, recibir o compartir electrones para alcanzar la estabilidad del gas noble más cercano, según la teoría de Kössel y Lewis.

Una molécula parece, a simple vista, un conjunto bien organizado de átomos que “deciden” permanecer unidos. En realidad, esa unión es el resultado de un delicado juego entre electrones que buscan alcanzar un estado de estabilidad similar al de los gases nobles. Esta tendencia a completar su último nivel energético explica por qué el sodio entrega un electrón, por qué el cloro lo acepta y por qué el carbono prefiere compartirlos. Sin embargo, aquí surge un punto intrigante: incluso los gases nobles, que ya tienen su octeto completo, pueden formar compuestos en condiciones adecuadas. Este hecho rompe la idea de que “no reaccionan nunca” y obliga a mirar más a fondo las interacciones electrónicas. Analizar las teorías de Kössel y Lewis permite comprender cómo se construyen los enlaces iónicos y covalentes, y por qué las moléculas no son simples uniones estáticas, sino estructuras dinámicas sustentadas por principios energéticos universales.
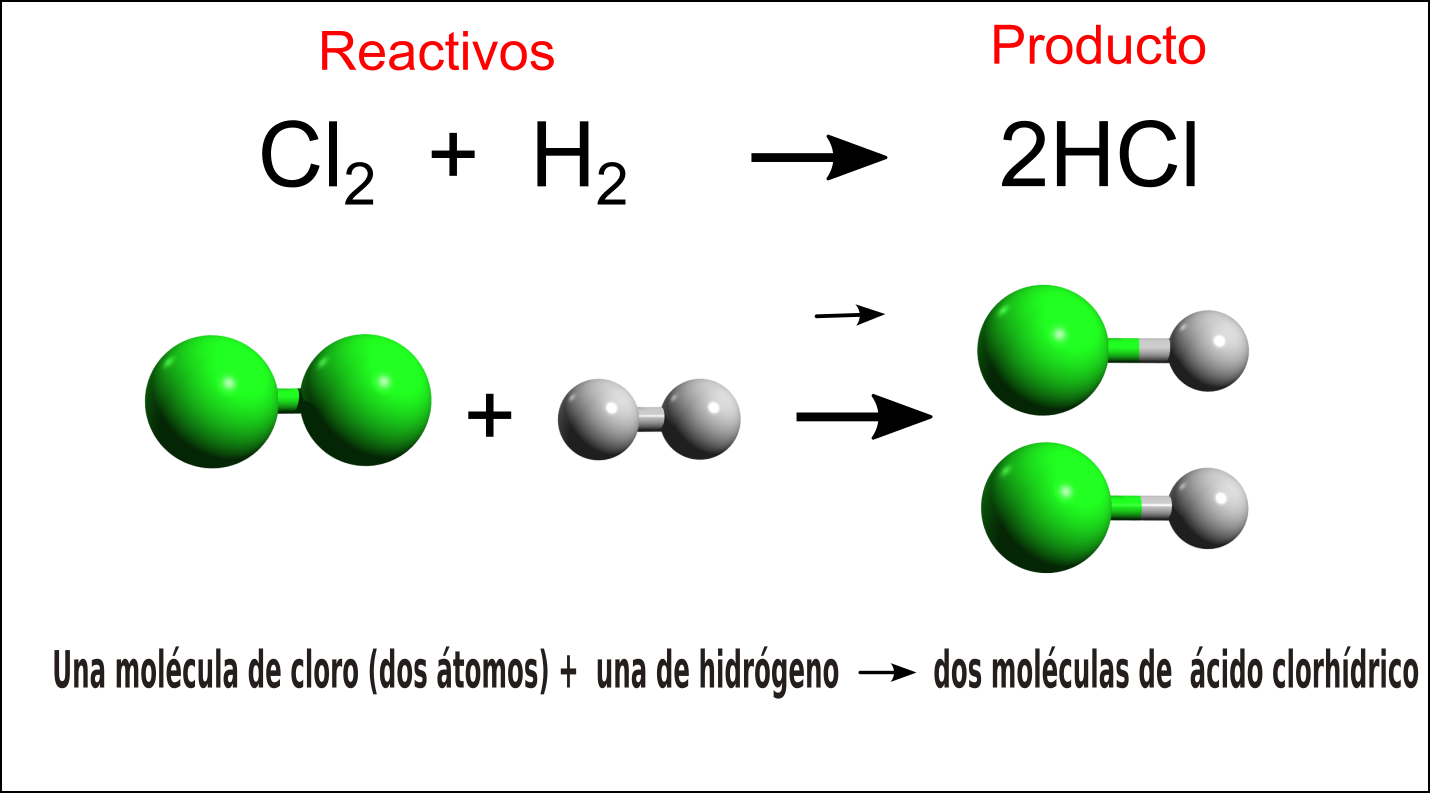
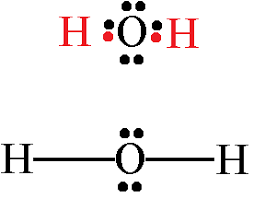

Estructuras de Lewis o estructura electrón-punto
Gilbert Lewis utilizó estructuras para explicar cómo actúan los átomos con sus electrones de valencia (los e que se hallan en el último nivel de energía) cuando forman un enlace químico y logran completar 8e.
Pasos para realizar las estructuras de Lewis
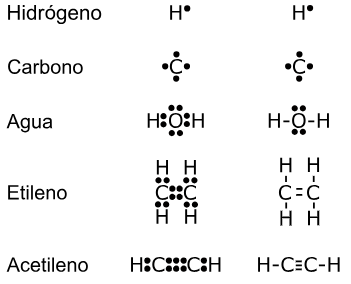
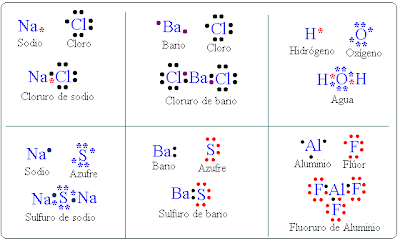
Adentrarse en el estudio de los enlaces químicos es aprender a leer el lenguaje con el que los átomos negocian su estabilidad. Cada cesión, cada ganancia y cada par compartido de electrones revela un patrón que se repite en minerales, proteínas, materiales tecnológicos y en la atmósfera misma. Las estructuras de Lewis, los enlaces iónicos, covalentes y las fuerzas intermoleculares abren una puerta hacia una comprensión más profunda de cómo se organiza la materia. Seguir explorando este campo conduce a descubrir cómo pequeñas modificaciones en las interacciones electrónicas pueden transformar las propiedades de un material o explicar procesos biológicos esenciales. El estudio continúa expandiéndose hacia la energía, la reactividad y la construcción de nuevos compuestos, siempre con la promesa de encontrar una lógica más amplia detrás de la diversidad química del mundo.