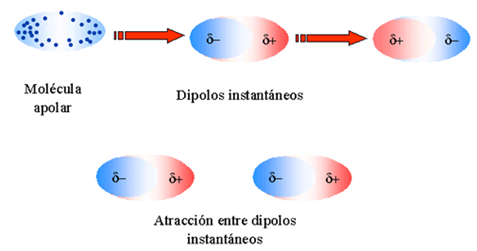
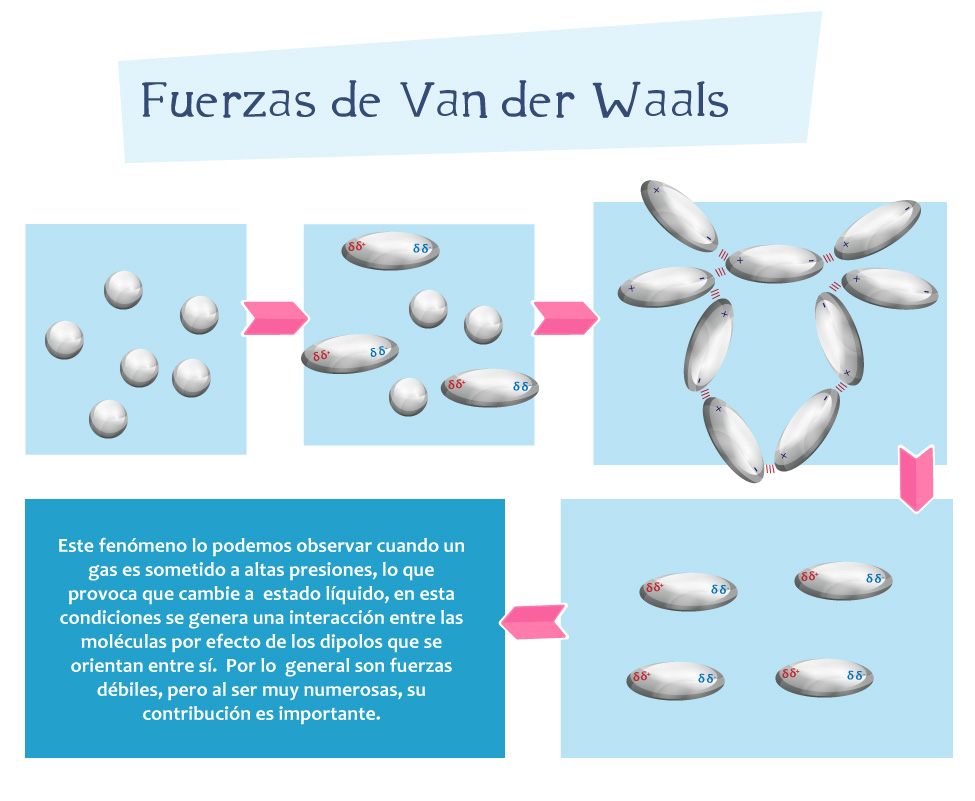
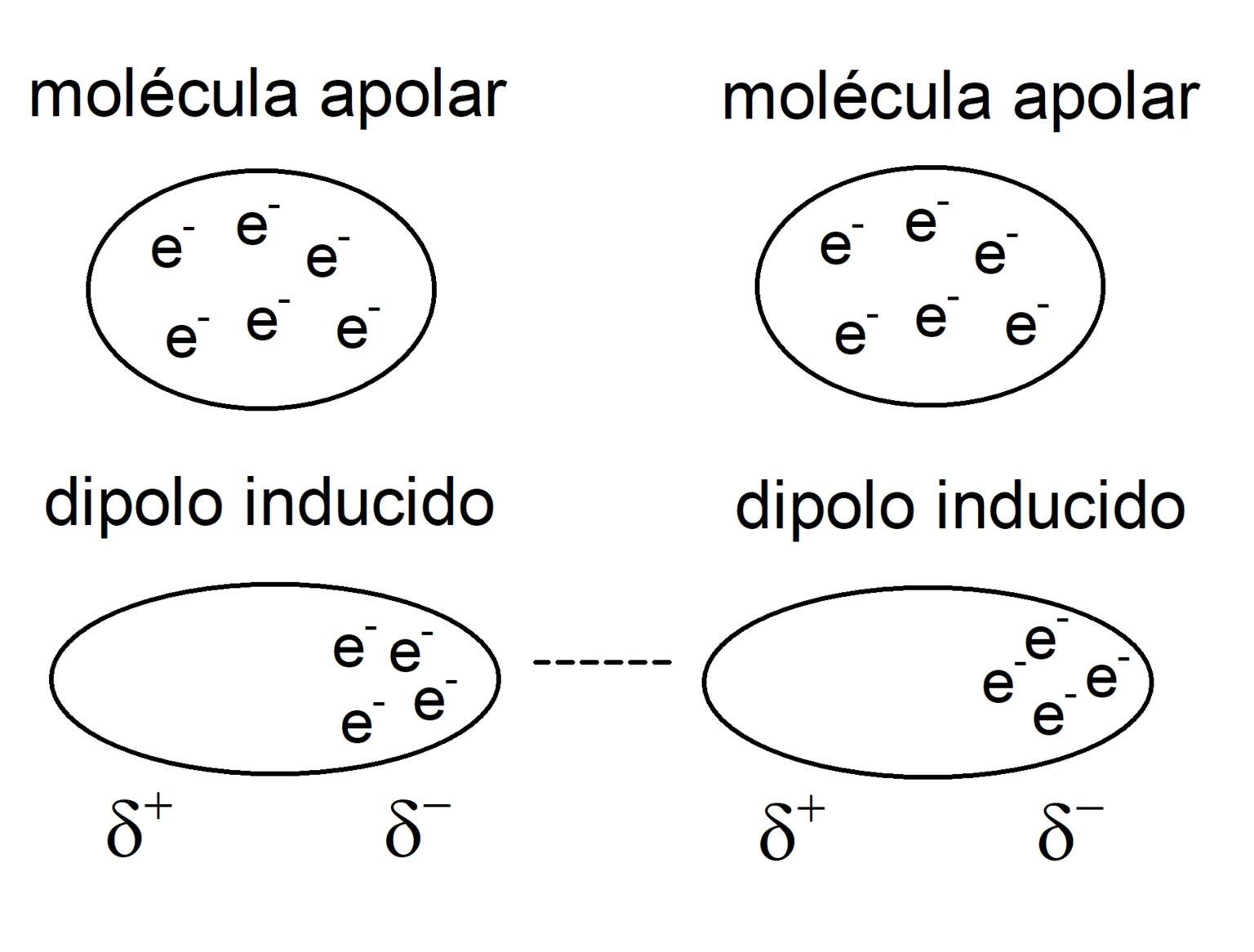Fuerzas intermoleculares
CN.Q.5.1.11. Establecer y diferenciar las fuerzas intermoleculares partiendo de la descripción del puente de hidrógeno, fuerzas de London y de Van der Walls, y dipolo-dipolo

Cuando observamos una gota de agua adherirse al vidrio, un insecto caminar sobre su superficie o un gas expandirse y llenar por completo un recipiente, solemos describir estos fenómenos sin pensar en las fuerzas invisibles que los gobiernan. Sin embargo, a escala molecular, nada ocurre al azar. Existen fuerzas de atracción entre moléculas que, aunque mucho más débiles que los enlaces químicos, determinan propiedades esenciales de la materia, como el estado físico, la solubilidad y la temperatura de ebullición. ¿Por qué algunas sustancias se mantienen unidas sin compartir electrones? ¿Cómo es posible que moléculas neutras se atraigan entre sí? Comprender las fuerzas intermoleculares implica aceptar que la estabilidad de la materia no depende solo de enlaces fuertes, sino también de interacciones sutiles que actúan de manera colectiva y constante.
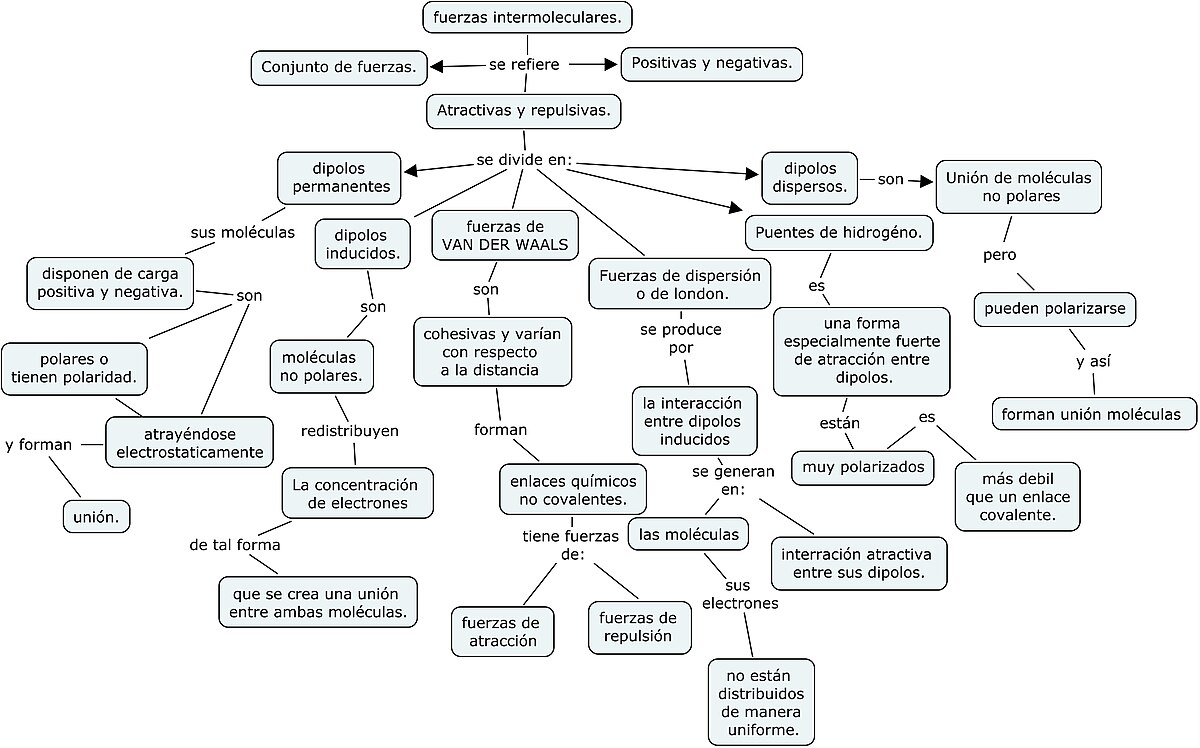
Fuerzas de atracción intermoleculares
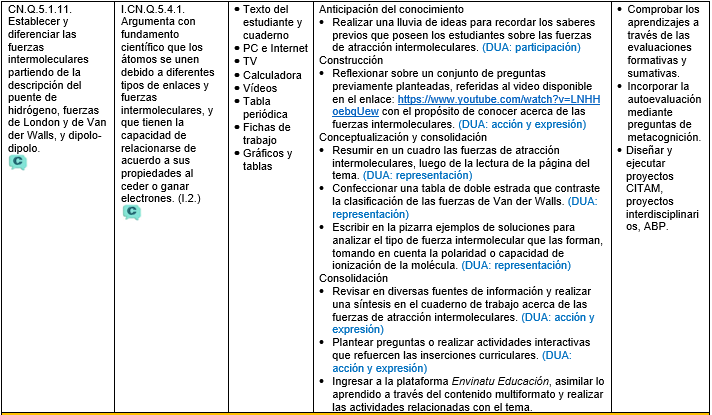
Atracción ion-ion
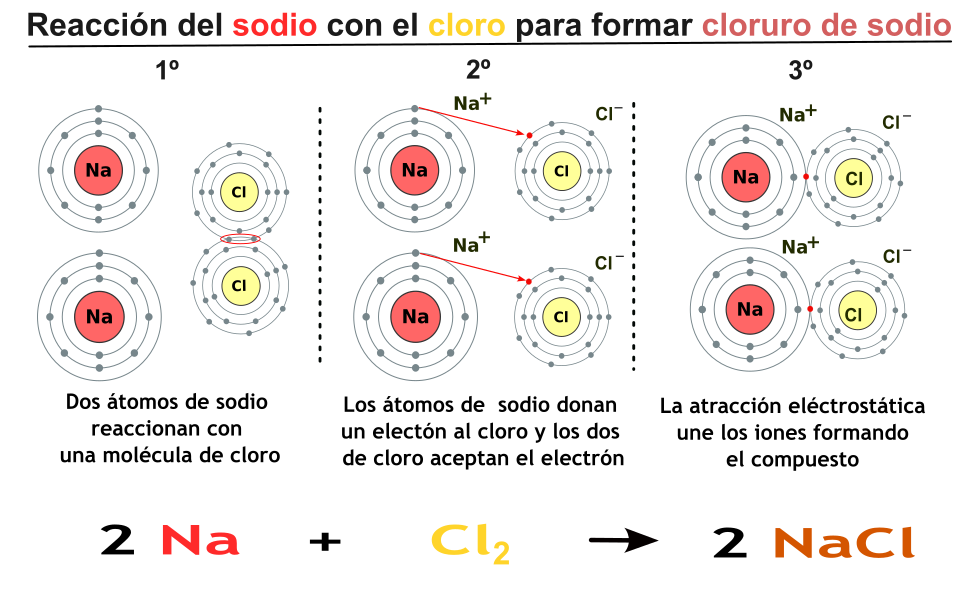
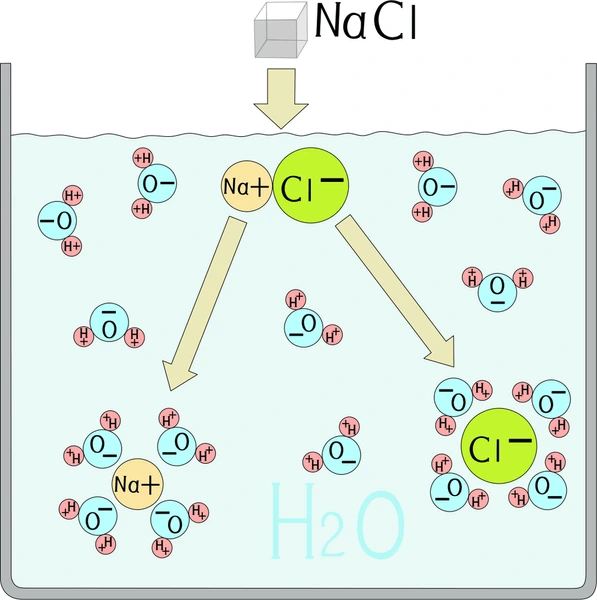
Atracción ion-dipolo
Fuerzas de Van der Walls
Se clasifican en tres:
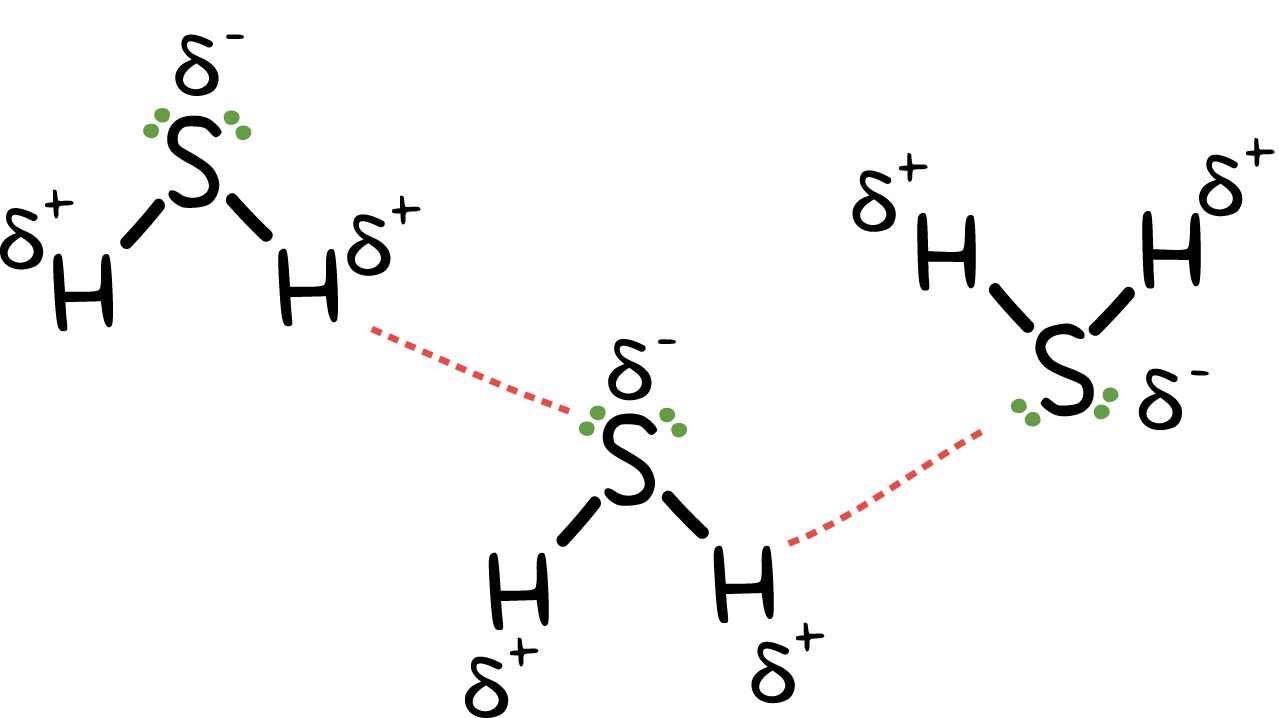
Atracción dipolo-dipolo

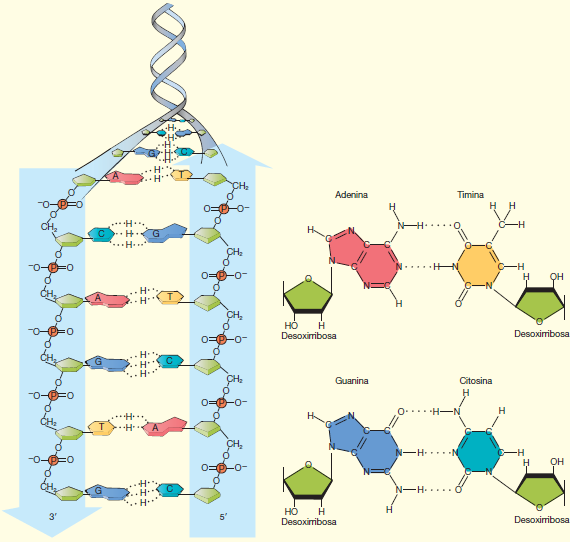
Atracción dipolo-dipolo inducido
Atracción con fuerzas de dispersión o de London
El estudio de las fuerzas intermoleculares revela que la materia se organiza en función de interacciones que responden a la estructura electrónica, la polaridad y la distribución de cargas en los átomos y moléculas. El puente de hidrógeno, las fuerzas dipolo-dipolo y las fuerzas de London muestran que incluso diferencias mínimas en la electronegatividad o en la movilidad de los electrones pueden generar efectos macroscópicos observables. Estas fuerzas explican por qué los átomos y las moléculas no solo se unen mediante enlaces químicos, sino que también se relacionan dinámicamente según su capacidad de ceder o atraer electrones. Reconocer este entramado de interacciones amplía la comprensión de la materia y sienta las bases para interpretar procesos biológicos, químicos y tecnológicos. En ciencia, cada fuerza descrita no cierra el conocimiento, sino que abre nuevas conexiones para entender cómo lo microscópico da forma al mundo que percibimos.