Las reacciones químicas y sus ecuaciones: masa atómica
CN.Q.5.2.10. Calcular y establecer la masa molecular de compuestos simples a partir de la masa atómica de sus componentes, para evidenciar que estas medidas son inmanejables en la práctica y que por tanto es necesario usar unidades de medida mayores, como el mol.

Imagina que quisieras pesar una sola molécula de agua. Sería como intentar medir el peso de una mota de polvo con una balanza para camiones: totalmente inútil. Las moléculas son tan pequeñas y tan ligeras que cualquier intento de manipularlas individualmente se vuelve absurdo desde el punto de vista práctico. Sin embargo, cada una tiene una masa molecular bien definida, determinada por las masas atómicas de sus elementos. El problema no es conceptual; el problema es de escala.
Cuando sumas las masas atómicas de hidrógeno y oxígeno para obtener la masa molecular del agua, obtienes un número que parece razonable sobre el papel, pero en realidad estás describiendo algo que ningún instrumento puede pesar de manera directa. Para trabajar con la materia tal como se presenta en el mundo cotidiano —en gotas, en gramos, en volúmenes— la ciencia se vio obligada a crear una unidad más grande, más manejable, capaz de agrupar cantidades astronómicas de moléculas: el mol.
A lo largo de esta actividad vamos a calcular masas moleculares de compuestos simples y veremos cómo esos valores, aunque matemáticamente correctos, se vuelven inviables para cualquier medición práctica. Esa incomodidad intelectual es justamente el indicio de que necesitamos una herramienta conceptual más grande y elegante para operar con la materia en cantidades reales.
Luego de Rutherford y de Bohr, en el ambiente científico se admitía que el átomo estaba constituido por un núcleo y una nube electrónica. Además, se sabía que el átomo era eléctricamente neutro, es decir, el número de protones (cargas positivas) era igual al número de electrones (cargas negativas). El número atómico (Z), correspondía a la cantidad de protones que presentaba un átomo determinado. La masa de un protón era igual a la masa de un núcleo de hidrógeno, y la masa de un electrón era despreciable en comparación con la masa de un protón.
Posteriores estudios del núcleo atómico pusieron de manifiesto algunas inquietudes:
La masa medida del núcleo de los átomos no coincidía con la masa de los protones correspondientes al número atómico: existía un exceso de masa.
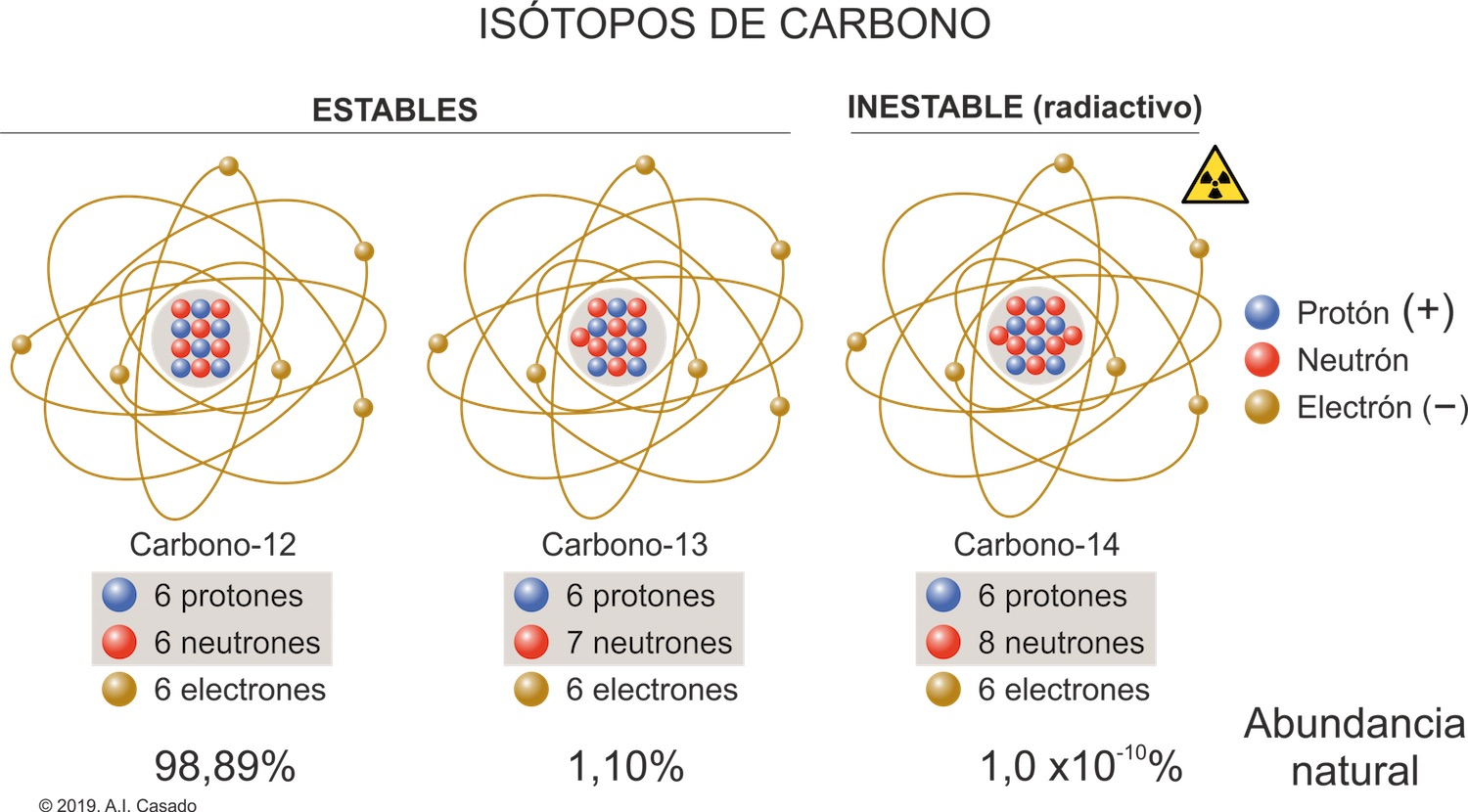
Existían átomos de los mismos elementos que podían presentar núcleos con diferente masa: los isótopos

En un átomo se reconocen tres partículas básicas cuya presencia determina su estructura y comportamiento. El electrón se encuentra en la envoltura y posee carga negativa; su masa es extremadamente pequeña, del orden de nueve coma once por diez a la menos veintiocho gramos, lo que equivale aproximadamente a una mil ochocientas cuarentaava parte de la masa de un protón. En el núcleo se localizan el protón y el neutrón. El protón tiene carga positiva y una masa cercana a uno coma seis siete tres por diez a la menos veinticuatro gramos, lo que corresponde a una unidad de masa atómica. El neutrón, también en el núcleo, no tiene carga eléctrica y su masa es prácticamente igual a la del protón, alrededor de uno coma seis siete cinco por diez a la menos veinticuatro gramos. Esta disposición, con electrones muy ligeros orbitando alrededor de un núcleo denso y estable, sustenta la estructura del átomo y permite comprender sus propiedades químicas y físicas.
Por lo tanto, quedó claro que el núcleo atómico estaba conformado por protones y neutrones, a los cuales se los considera nucleones. La suma del número de neutrones y protones del núcleo atómico se conoce como número de masa (A)
Para poder medir una masa extremadamente pequeña de un núcleo atómico se ha tomado como referencia una doceava parte del átomo de carbono 12. Es decir, una unidad de masa atómica denominada Dalton (Da) equivale a un doceavo de porciones de materia de carbono 12.
La relación se entiende mejor si se comienza con un caso sencillo. Cuando un átomo posee seis protones y ocho neutrones, el carbono, basta con sumar estas dos cantidades para obtener un total de catorce nucleones, de modo que su número de masa es catorce. En un núcleo más grande, como aquel formado por noventa y dos protones y ciento cuarenta y seis neutrones, del uranio, la suma asciende a doscientos treinta y ocho nucleones, lo que se expresa como número de masa doscientos treinta y ocho. Este procedimiento permite visualizar cómo el tamaño del núcleo depende directamente de la cantidad de nucleones que lo componen y facilita comparar átomos ligeros con otros mucho más pesados.
Al calcular la masa molecular de diferentes compuestos, descubriste dos cosas fundamentales. La primera es que la estructura de la materia puede expresarse con precisión: basta con conocer las masas atómicas de los elementos para determinar la masa de una molécula. La segunda es que, cuando hablamos de entidades tan pequeñas, los números dejan de tener sentido práctico. No podemos pesar una molécula, ni cien, ni mil.
La introducción del mol fue una solución brillante a este problema. Permite relacionar el mundo microscópico con el macroscópico, conectar el comportamiento de átomos y moléculas con las cantidades de materia que podemos manipular en un laboratorio o en la vida diaria. Cada vez que usas el mol, estableces un puente entre escalas: desde lo imperceptible hasta lo tangible.
Esa idea —crear herramientas conceptuales capaces de traducir universos distintos— es una de las fuerzas más elegantes de la ciencia. La comprensión del mol no es solo un ejercicio numérico; es un recordatorio de que el conocimiento avanza cuando encontramos formas de hacer visible lo invisible. Esta perspectiva abre el camino hacia la estequiometría, las reacciones químicas y la comprensión cuantitativa de la materia en todas sus formas.