Propiedades físicas de los compuestos covalentes
CN.Q.5.3.1. Examinar y clasificar las características de los distintos tipos de sistemas dispersos según el estado de agregación de sus componentes y el tamaño de las partículas de la fase dispersa.
CN.Q.5.1.10. Deducir y explicar las propiedades físicas de compuestos iónicos y covalentes desde el análisis de su estructura y el tipo de enlace que une a los átomos, así como de la comparación de las propiedades de sustancias comúnmente conocidas

A primera vista, todas las moléculas podrían parecer simples combinaciones de átomos unidos entre sí. Sin embargo, basta formular una pregunta aparentemente inocente para abrir una grieta en esa idea: ¿qué molécula es más compleja, el metano o una proteína? El metano está formado por un solo átomo de carbono y cuatro de hidrógeno; una proteína, en cambio, puede contener miles de átomos organizados en una estructura tridimensional altamente específica. Pero la complejidad no depende solo del tamaño o del número de átomos, sino también del tipo de enlaces, de la disposición espacial y de las interacciones con el entorno.
Esta reflexión nos conduce a otro interrogante clave: ¿por qué el agua, una molécula tan pequeña, se encuentra en estado líquido en condiciones normales, mientras que otras moléculas de tamaño similar son gases? La respuesta no está en la masa de la molécula, sino en una propiedad fundamental: la polaridad. La distribución desigual de cargas eléctricas en el agua permite que sus moléculas se atraigan entre sí, generando interacciones que modifican profundamente su comportamiento físico. Comprender estas ideas exige revisar lo que ya sabemos y, al mismo tiempo, aceptar que algunas intuiciones cotidianas deben ser cuestionadas.
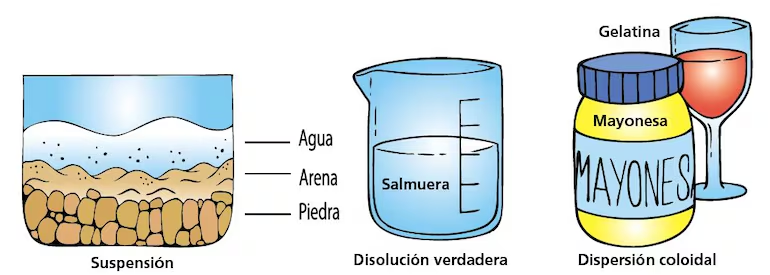
La forma de las moléculas de un enlace covalente
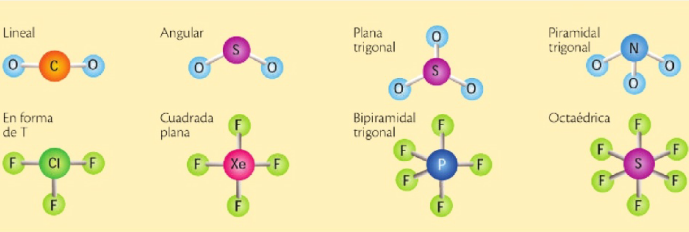
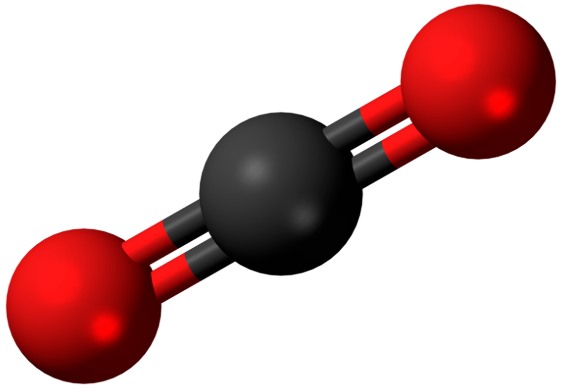
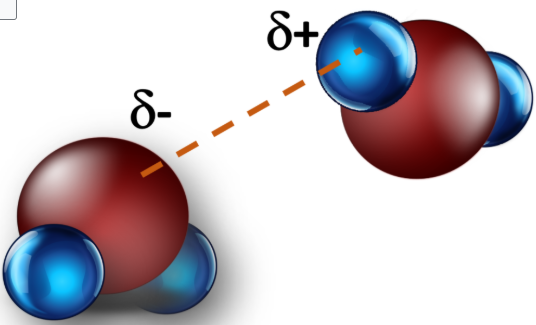
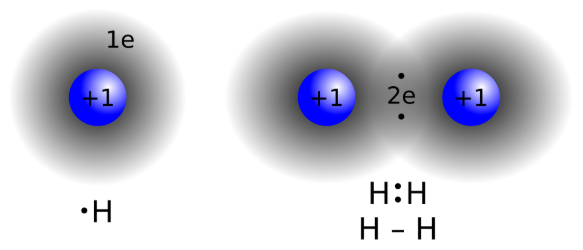
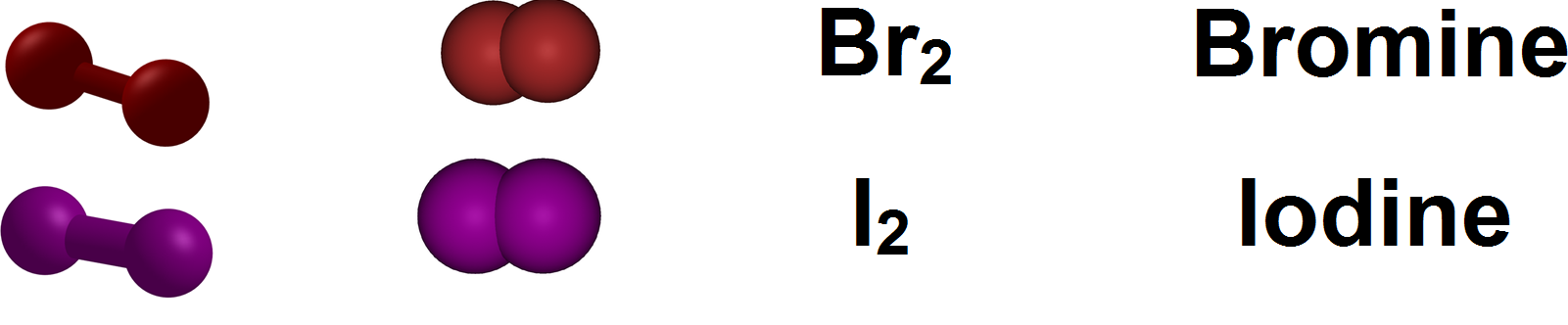

Estos ejemplos ilustran el hecho de que el estado de agregación no depende de una sola propiedad, sino del balance entre polaridad, masa molecular y tipo de interacciones intermoleculares.
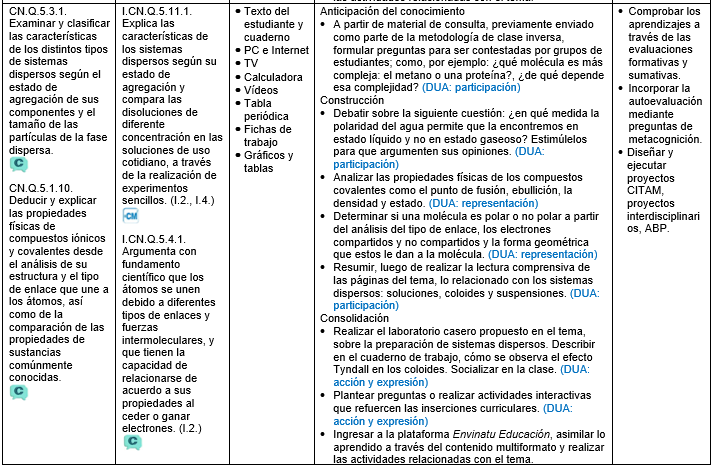
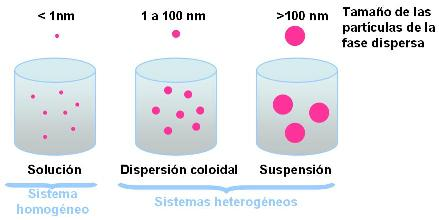
Sistemas dispersos: soluciones, coloides y suspensiones
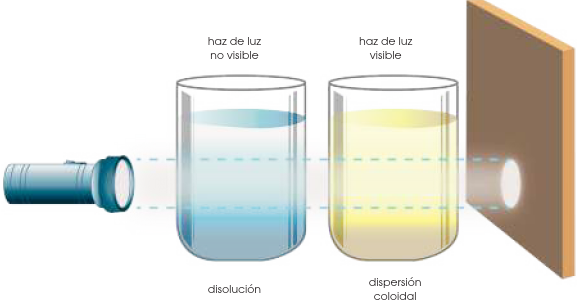
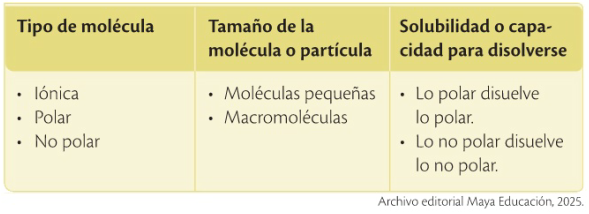
Los sistemas dispersos se muestran homogéneos y pueden presentarse en todos los estados de agregación.

Competencia matemática. Cuando tenemos una suspensión, podemos observar que con el tiempo, si se la deja en reposo, la fase dispersa se decanta o sedimenta. La velocidad con la que esto sucede depende del tamaño y peso de las partículas de la fase dispersa y de las características de la fase dispersante. Mientras mayor tamaño tengan las partículas, tendrán un mayor peso y se decantarán más rápido. ¿Esta es una relación directa o indirectamente proporcional?