graph TD
A[🪐 TEORÍA DE BOHR<br/>Modelo Atómico Cuántico] --> B[⚛️ FÍSICA CLÁSICA<br/>Newton + Electrodinámica de Maxwell]
A --> C[🔬 FÍSICA CUÁNTICA<br/>Hipótesis de Planck]
B --> D[✅ CONDICIÓN:<br/>Átomo ESTABLE<br/>No emite radiación<br/>No libera fotones<br/><br/>📊 Estado: Órbita fija]
C --> E[🌟 CONDICIÓN:<br/>Átomo ACTIVO<br/>Emite/Absorbe radiación<br/>Espectros luminosos<br/><br/>🎯 Salto cuántico entre órbitas]
style A fill:#1565c0,color:#ffffff,stroke:#0d47a1,stroke-width:3px
style B fill:#2e7d32,color:#ffffff,stroke:#1b5e20,stroke-width:2px
style C fill:#6a1b9a,color:#ffffff,stroke:#4a148c,stroke-width:2px
style D fill:#ff9800,color:#000000,stroke:#ef6c00,stroke-width:2px
style E fill:#c2185b,color:#ffffff,stroke:#880e4f,stroke-width:2px
Modelo atómico: modelo mecánico-cuántico de la materia (1)
CN.Q.5.1.5. Observar y aplicar el modelo mecánico-cuántico de la materia en la estructuración de la configuración electrónica de los átomos considerando la dualidad del electrón, los números cuánticos, los tipos de orbitales y la regla de Hund.

La luz parece algo cotidiano: ilumina la habitación, revela colores, delimita formas. Sin embargo, cuando se observa con detenimiento, comienza a comportarse como un fenómeno sorprendente. ¿De qué está hecha realmente? Si se la piensa como una onda, se desplaza sin necesidad de un medio; si se la considera como partículas llamadas fotones, transporta paquetes discretos de energía. En ambos casos, la luz desafía la intuición. Incluso los colores, que parecen tan obvios, esconden un comportamiento físico complejo. Por ejemplo, el negro no es un color en el sentido estricto del espectro: es la ausencia de luz reflejada. Esa ausencia se interpreta como un “color” sólo porque el cerebro traduce la falta de señales en una experiencia visual coherente. Empezar a cuestionar estos detalles abre la puerta para comprender cómo se comportan los electrones, por qué requieren números cuánticos para describirse y cómo la materia revela su estructura cuando se la observa a escalas diminutas. Cada misterio inicial se convierte en una invitación a mirar el átomo con nuevos ojos.
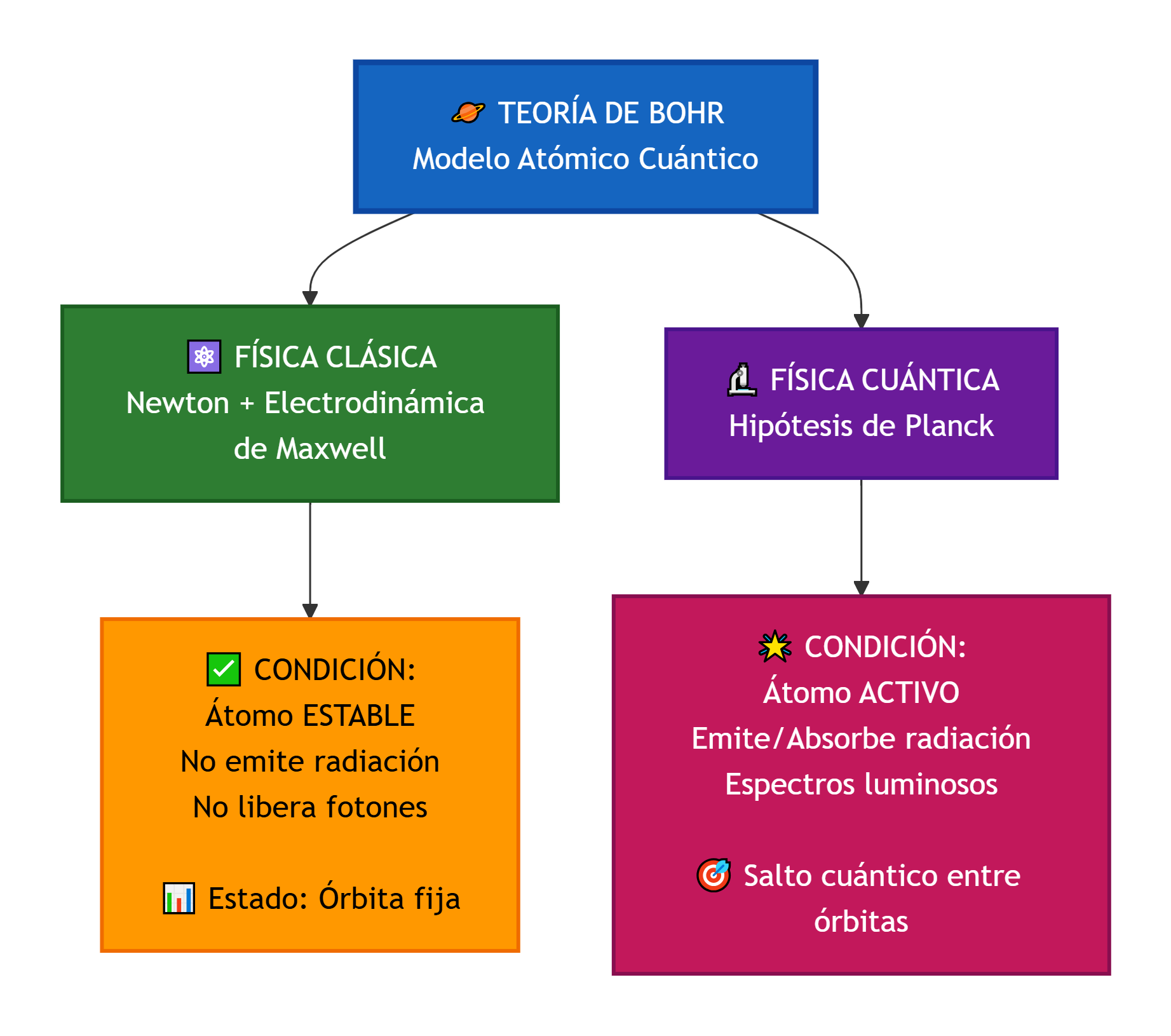
El artículo que Bohr escribió en 1913, explicando su modelo atómico, no fue bien recibido por la comunidad científica; el mismo Thomson difería con las ideas propuestas por Bohr: “parece necesario introducir en las leyes en cuestión una cantidad extraña a la electrodinámica clásica, es decir, la constante de Planck, o los cuantos elementales de acción como frecuentemente se llama”.
La Mecánica cuántica nació con Bohr, quien comprendió que las leyes clásicas de la Física no podían explicar de forma adecuada la estructura de un átomo nuclear; por tanto, tuvo que fusionar viejas ideas de la Mecánica de Newton con las nuevas propuestas de Planck y sus cuantos.
Aunque en principio esta mezcla de ideas expuestas por Bohr estaba incompleta y en parte errada, sirvió de base para posteriores investigaciones.
Principio de complementariedad
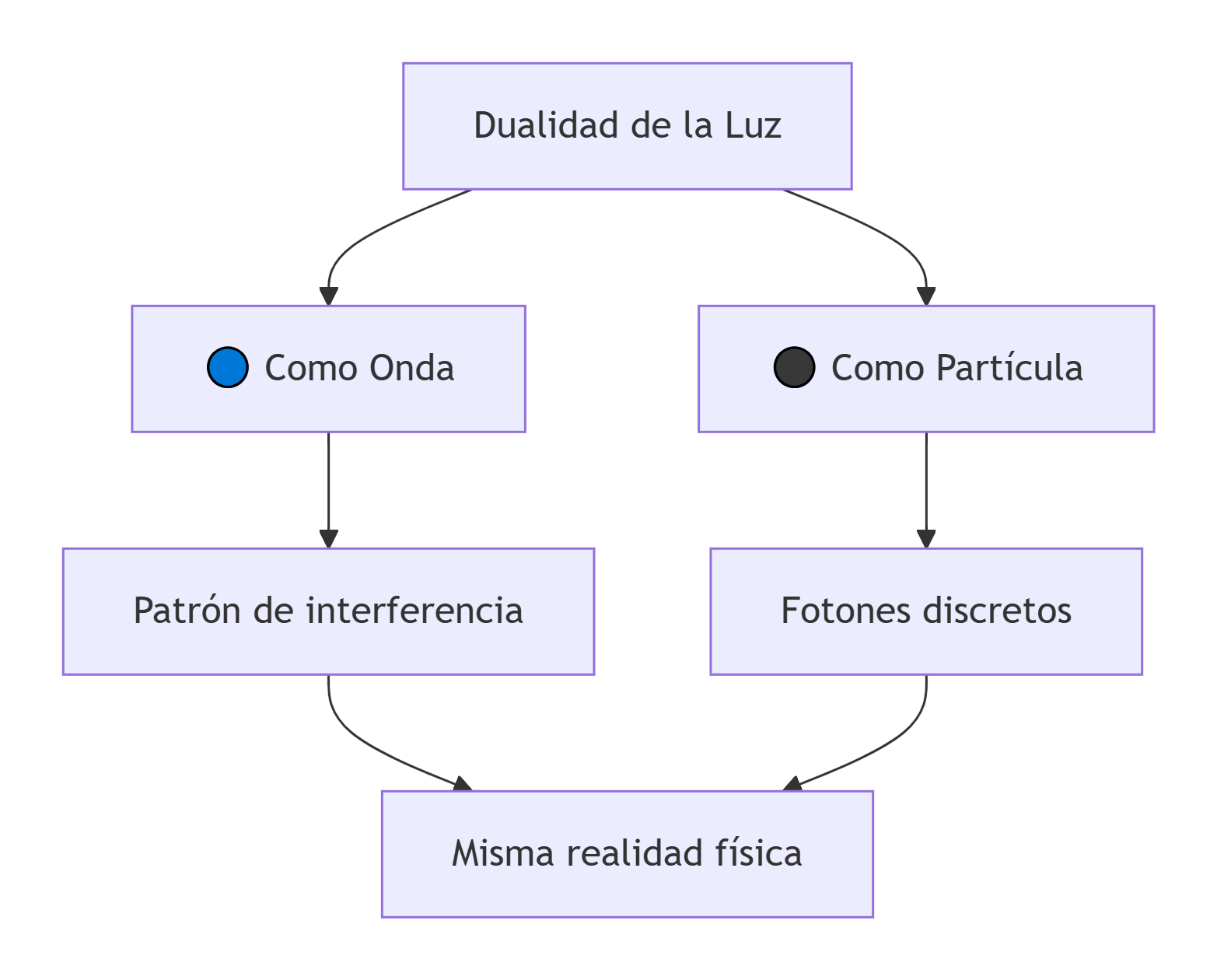
Albert Einstein era partidario de los fotones. Luego de sus investigaciones con rayos X, concluyó que la luz, cuando viaja a través de un medio, se comporta como ondas ocupando todo el espacio, y, cuando lo hace en el espacio vacío o choca contra un cuerpo, se comporta como partícula. Bohr llamo a esta propiedad onda-partícula “ principio de complementariedad ”. Así nace la Mecánica cuántica, que se encarga de explicar cómo funciona el universo con objetos y espacios más pequeños que un átomo.
Estrategia para resolver problemas. Cuando te enfrentes a un problema de química, debes seguir algunos pasos importantes. Comprender el problema. Si no lo comprendes, no vas a poder resolverlo. Para tener éxito, te recomendamos lo siguiente: leer adecuadamente el problema y replantearlo con tus propias palabras.
La dualidad del electrón
La teoría de la relatividad de Einstein manifestaba que la materia era una forma concentrada de energía que se puede calcular mediante la fórmula:
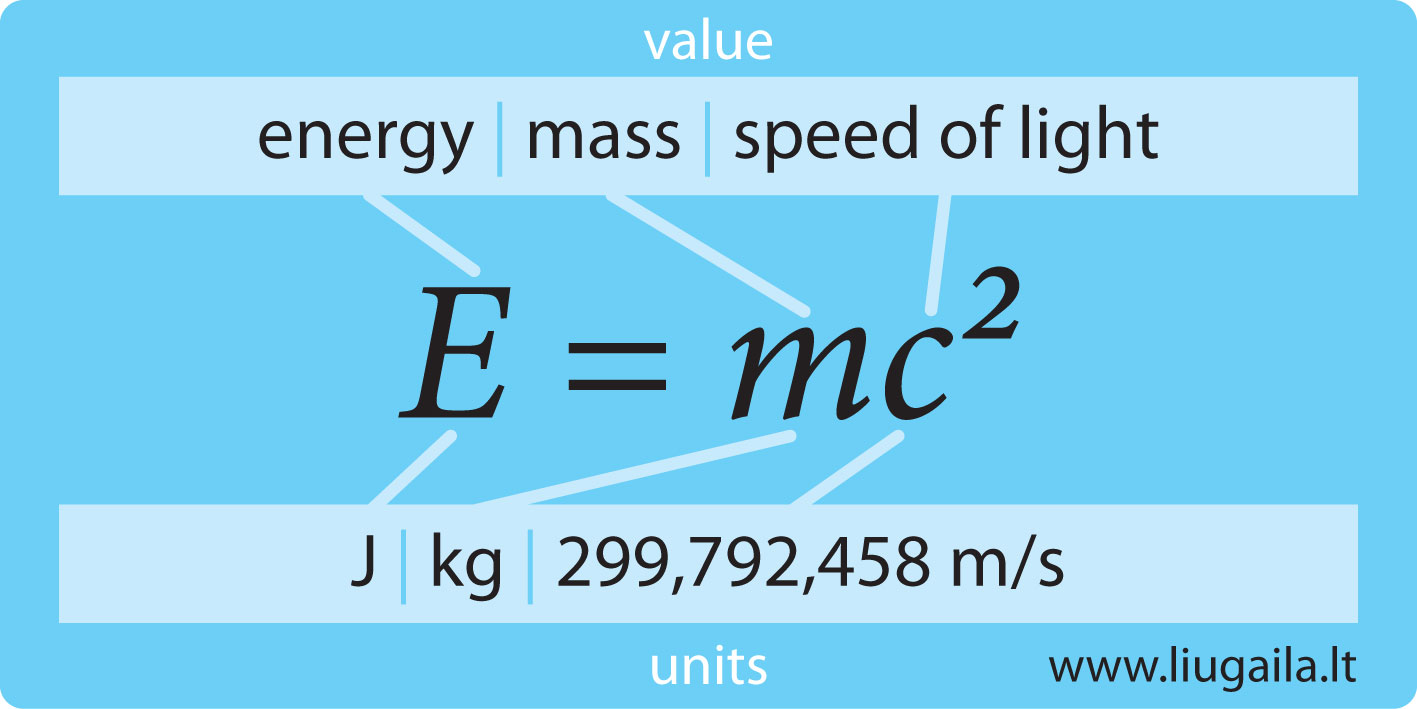
El científico Louis de Broglie (Francia, 1892-1987), luego de analizar la teoría de Einstein, propuso que, si la materia es energía y si la luz era a la vez onda y partícula, el electrón, que era una partícula, podía también ser una onda. Es decir, el electrón, por poseer masa y movimiento, se comporta como un corpúsculo, pero también tiene una longitud de onda, por eso puede difractarse, es decir, aparecer en varias regiones del espacio al mismo tiempo.
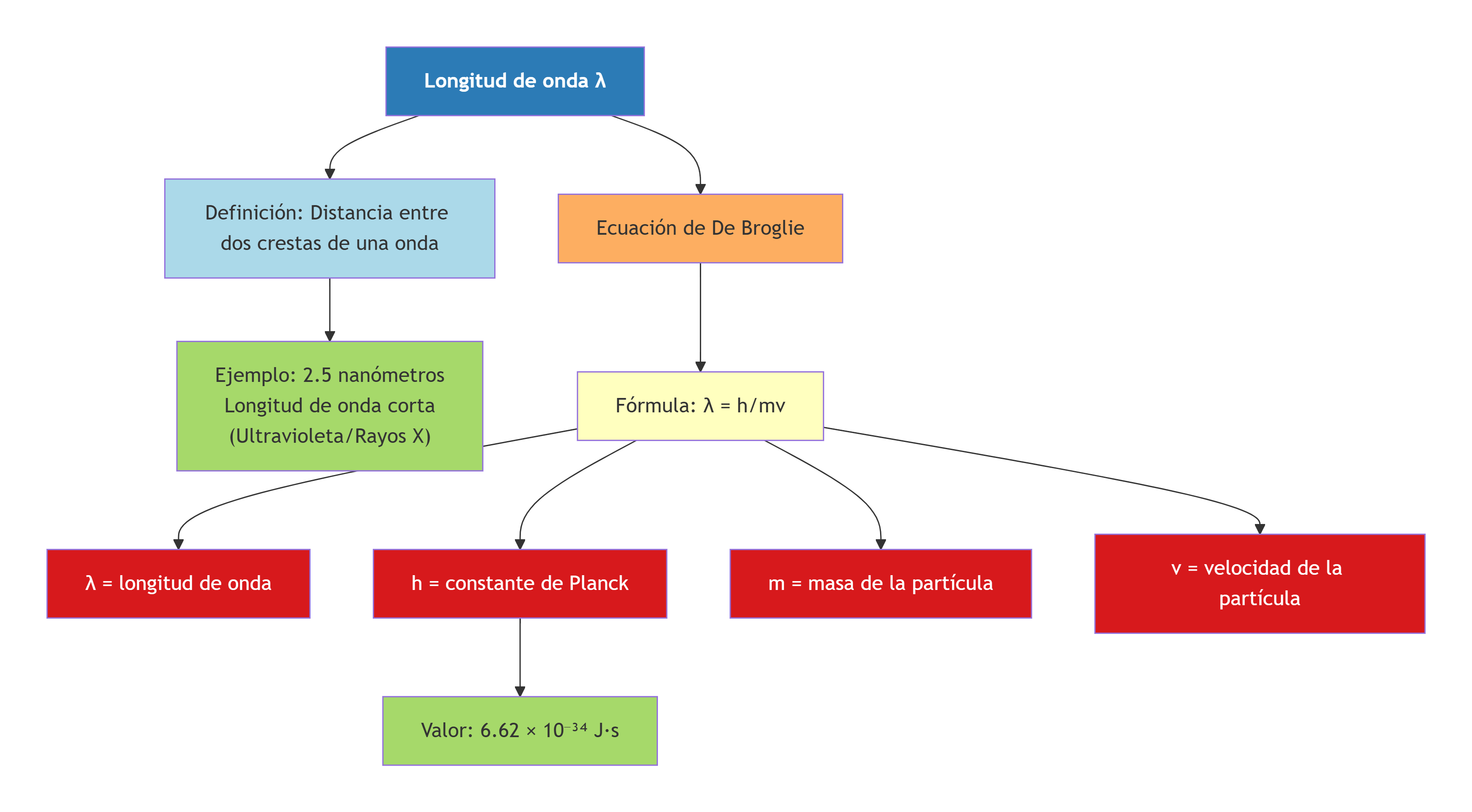
Broglie extendió esta propiedad de onda-partícula a todas las partículas subatómicas, y proporcionó la ecuación con la cual se puede medir su longitud de onda.
graph TD
node1[Longitud de onda λ]
node1 --> node2[Definición: Distancia entre dos crestas de una onda]
node1 --> node3[Ecuación de De Broglie]
node2 --> node4[Ejemplo: 2.5 nanómetros<br/>Longitud de onda corta<br/>(Ultravioleta/Rayos X)]
node3 --> node6[Fórmula: λ = h/mv]
node6 --> node7[λ = longitud de onda]
node6 --> node8[h = constante de Planck]
node6 --> node9[m = masa de la partícula]
node6 --> node10[v = velocidad de la partícula]
node8 --> node11[Valor: 6.62 × 10⁻³⁴ J·s]
style node1 fill:#2c7bb6,color:white,font-weight:bold
style node2 fill:#abd9e9
style node3 fill:#fdae61
style node4 fill:#a6d96a
style node6 fill:#ffffbf
style node7 fill:#d7191c,color:white
style node8 fill:#d7191c,color:white
style node9 fill:#d7191c,color:white
style node10 fill:#d7191c,color:white
style node11 fill:#a6d96a
Principio de incertidumbre
En 1926, el físico alemán Werner Heisenberg (1901-1976) sostuvo que la doble naturaleza de la materia limita determinar con exactitud y de forma simultánea la posición y energía de un electrón en un instante específico. Únicamente se puede considerar la probabilidad de encontrar el electrón en cierta región del espacio que rodea al núcleo. Por consiguiente, no es apropiado imaginar los electrones en movimiento en órbitas definidas, como pensaba Bohr.
Los orbitales son regiones de espacio alrededor de un núcleo atómico donde hay mayor probabilidad de encontrar un electrón. El electrón ocupa todo ese espacio en el mismo momento.
Los números cuánticos
Para los científicos estaba claro que la dualidad onda-partícula del electrón mostraba que no se hallaban girando alrededor del núcleo en órbitas planas, sino que vibraban en espacios tridimensionales 3D, a los que se les dio el nombre de orbitales
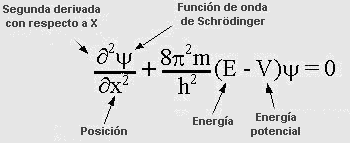
Erwin Schrödinger (Austria, 1887-1961) se propuso encontrar la manera de relacionar la energía que tienen el electrón, como partícula con masa, con la onda que describe en su orbital, y para esto incorporó un descriptor matemático o función de onda (psi) en una ecuación que describe el comportamiento energético de las partículas subatómicas.
Función de onda = descriptor matemático de comportamiento dual, orbital
El cuadrado de la función de onda = zona con mayor probabilidad de encontrar un electrón
Para describir la función de onda, solo se utilizan variables que usan números enteros. Estas variables se denominan números cuánticos y ellos nos permiten describir la forma tridimensional de los orbitales y su estado energético.
Schrödinger propuso tres números cuánticos: número cuántico principal (n), angular (l) y número cuántico magnético (m sub l). El cuarto número cuántico de spin (m sub s) fue propuesto después, cuando se conoció que en cada orbital podían encontrarse 2 electrones.
Números cuánticos
- Número cuántico principal, n
Determina el número de niveles de energía en un átomo. Puede tomar los valores uno, dos, tres, y así sucesivamente. Para los elementos conocidos se requieren siete niveles energéticos. El nivel menos energético corresponde a n igual a uno y el más energético corresponde a n igual a siete. A mayor valor de n, el electrón tiene mayor energía y está menos atado al núcleo. El número total de electrones en un nivel energético viene dado por la expresión dos n al cuadrado, en donde n corresponde al nivel de energía.
- Número cuántico secundario o azimutal, l
Determina los subniveles de energía que tiene cada nivel. Su valor depende del número cuántico principal. Puede tomar valores desde cero hasta n menos uno. A cada valor del número cuántico azimutal le corresponde una forma de orbital que se identifica con una letra minúscula: s, de sharp; p, de principal; d, de difuso; y f, de fundamental.
- Número cuántico magnético, m sub l
Indica la orientación del orbital en el espacio. Toma valores enteros que van desde menos l hasta más l, incluyendo el cero. En general, el número de orbitales de un subnivel dado es igual a dos l más uno.
- Número cuántico de spin, m sub s
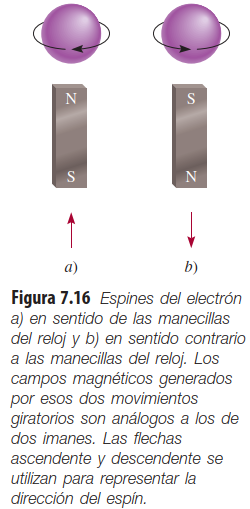
Ecuación de Schrödinger