Sistemas dispersos: soluciones electrolíticas o iónicas
CN.Q.5.3.1. Examinar y clasificar las características de los distintos tipos de sistemas dispersos según el estado de agregación de sus componentes y el tamaño de las partículas de la fase dispersa.
CN.Q.5.1.10. Deducir y explicar las propiedades físicas de compuestos iónicos y covalentes desde el análisis de su estructura y el tipo de enlace que une a los átomos, así como de la comparación de las propiedades de sustancias comúnmente conocidas.

Propiedades físicas de los compuestos iónicos
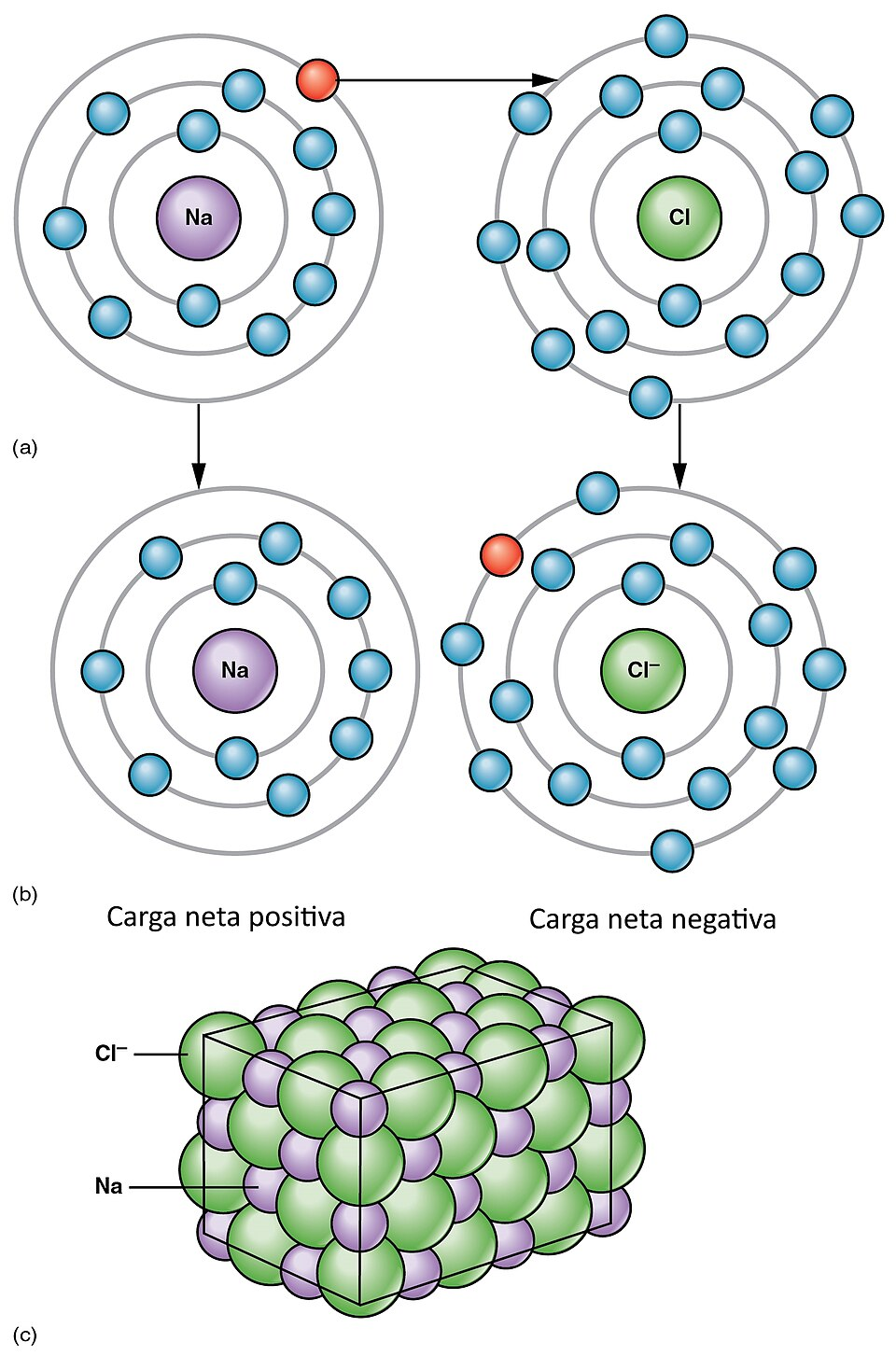

Los compuestos iónicos, al ser sólidos cristalinos, son duros y quebradizos, con puntos de fusión superiores a 300 grados centígrados, y puntos de ebullición superiores a 1000 grados centígrados. Son solubles en agua e insolubles en solventes no polares. Al estar disueltos en agua pueden conducir la corriente eléctrica. Debido a que sus iones se separan, por ello se los conoce como electrolitos.
Clasificación de los sistemas dispersos de acuerdo con el tamaño de la partícula de la fase dispersa
Sistemas dispersos: soluciones electrolíticas o iónicas
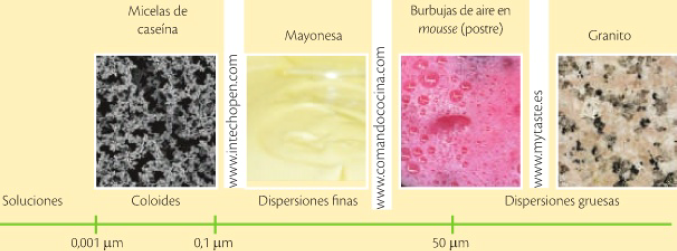
Los sistemas dispersos son mezclas donde una sustancia se encuentra difundida en otra. De acuerdo al tamaño de la partícula que se mezcla, se clasifican a estos sistemas en:
Dispersiones gruesas (mezclas heterogéneas)
Dispersiones finas (mezclas homogéneas)
Coloides (mezclas homogéneas)
Soluciones (mezclas homogéneas)
Los compuestos iónicos, al disolverlos en agua, se disocian, es decir, las moléculas se separan en sus iones. El tamaño de estos iones es tan pequeño que con el agua forma soluciones a las que se denominan iónicas o electrolíticas, producidas por la presencia de cargas positivas y negativas.
Veamos unos ejemplos:
El cloruro de sodio se separa en ion sodio con carga positiva e ion cloruro con carga negativa.
El bicarbonato de sodio se separa en ion sodio con carga positiva e ion bicarbonato con carga negativa.
En ambos casos, el metal origina el catión y el no metal origina el anión.
Interdisciplinariedad. Química y Biología. Los electrolitos cumplen con una función importante en los seres vivos: permiten transmitir señales y ayudan en el transporte de sustancias. Por eso la pérdida de electrolitos produce desequilibrio. El suero fisiológico es una solución que sirve para restablecer el equilibrio electrolítico de nuestro cuerpo.