Enlace metálico
CN.Q.5.1.10. Deducir y explicar las propiedades físicas de compuestos iónicos y covalentes desde el análisis de su estructura y el tipo de enlace que une a los átomos, así como de la comparación de las propiedades de sustancias comúnmente conocidas.

Cuando observamos un metal cotidiano —una moneda, un cable eléctrico o la superficie brillante de una herramienta— estamos viendo el resultado de un tipo de unión atómica que no se comporta como los enlaces iónicos ni como los enlaces covalentes. Dentro del metal, los átomos no permanecen unidos de manera rígida entre pares, sino que forman una estructura en la que los núcleos están ordenados y los electrones se desplazan de forma colectiva, casi como si fueran un “mar electrónico”. Esta organización microscópica explica fenómenos macroscópicos tan familiares como la conductividad eléctrica, el brillo metálico o la capacidad de deformarse sin romperse. Comprender cómo surge esta conducta desde la estructura del enlace abre la puerta a interpretar por qué los materiales se comportan como lo hacen y cómo la materia puede reorganizarse para crear propiedades nuevas. La ciencia de los enlaces es, en esencia, una ventana directa al comportamiento de la materia.

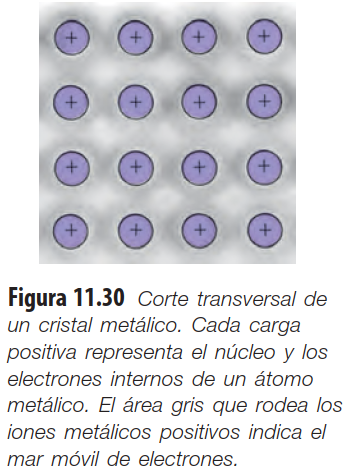

Características del enlace metálico



Interdisciplinariedad. Química e Historia. Los metales fueron unas de las primeras sustancia que pudo trabajar el ser humano. Su descubrimiento permitió el avance de la civilización debido a la invención de utensilios, herramientas y nuevas tecnologías de construcción.
El estudio del enlace metálico revela que los materiales no son simples objetos inertes, sino sistemas organizados cuyo comportamiento depende de interacciones profundas entre átomos y electrones. Cada propiedad —la dureza, la maleabilidad, la solidez de una estructura o la eficiencia de un conductor eléctrico— es la expresión visible de un orden microscópico que podemos analizar, comparar y predecir. Comprender cómo se enlazan los átomos permite reconocer patrones, explicar fenómenos y anticipar las características de nuevas sustancias. Continuar explorando estas interacciones abre caminos hacia la ingeniería de materiales, la nanotecnología y el diseño de soluciones para los desafíos actuales. La materia guarda aún muchos secretos, y cada enlace es una invitación a descubrirlos.